Proteinablagerungen bei Demenz beeinflussen Gehirnaktivitäten beim Schlafen
Alzheimer: Plaques stören Gedächtnisbildung im Schlaf
Vor allem die langsamen Schlafwellen, sogenannte slow oscillations, die unser Gehirn nachts erzeugt, dienen dazu, Gelerntes zu verfestigen und Erinnerungen in den Langzeitspeicher zu verschieben. Die Wellen werden über ein Netzwerk an Nervenzellen in der Hirnrinde gebildet und breiten sich dann in andere Hirnareale wie den Hippocampus aus.
„Diese Wellen sind eine Art Signal, mit dem sich die Hirnareale gegenseitig bestätigen `ich bin bereit, der Informationsaustausch kann losgehen`. Während des Schlafes herrscht daher ein hohes Maß an Kohärenz zwischen weit entfernten Nervenzellnetzwerken“, erklärt Dr. Dr. Marc Aurel Busche, Wissenschaftler an der Klinik und Poliklinik für Psychiatrie und Psychotherapie am TUM Klinikum rechts der Isar und am Institut für Neurowissenschaften der TUM. Er leitete gemeinsam mit Prof. Dr. Arthur Konnerth vom Institut für Neurowissenschaften die Studie, die in der Fachzeitschrift Nature Neuroscience erschien.
Gestörte Ausbreitung der Schlafwellen bei Alzheimer
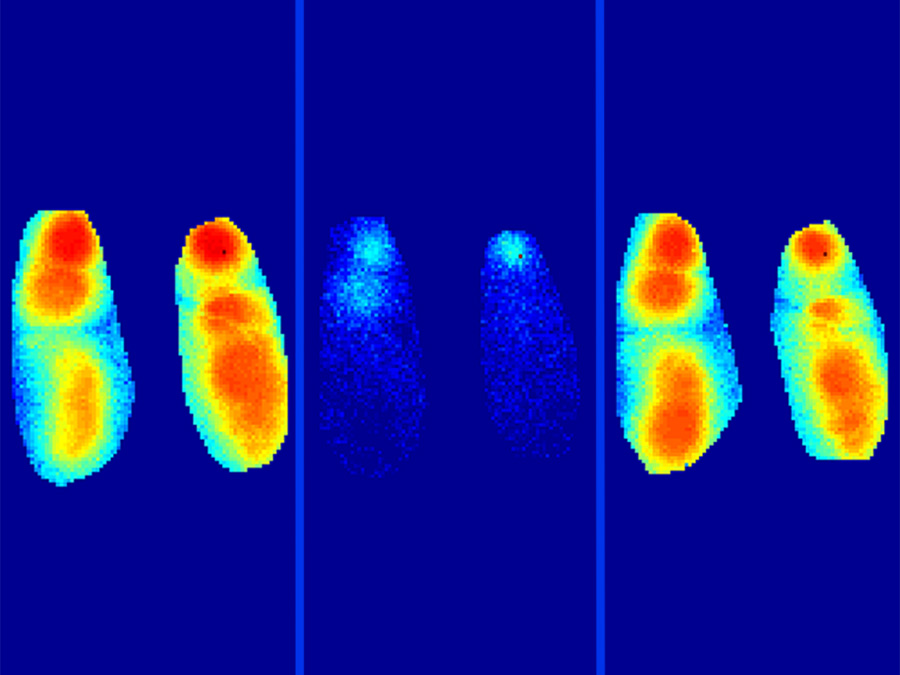
Wie die Forscher herausfanden, ist bei Alzheimer dieser Kohärenz-Prozess gestört. Sie nutzten für ihre Studie Mausmodelle, mit denen sich die Defekte im Gehirn bei Alzheimerkranken nachstellen lassen. Die Tiere bilden dieselben Proteinablagerungen, die so genannten β-Amyloid Plaques, die auch in Patienten sichtbar sind. Die Wissenschaftler konnten jetzt zeigen, dass diese Plaques direkt Störungen bei den langsamen Schlafwellen auslösen. „Die langsamen Oszillationen treten zwar noch auf, sie können sich aber nicht mehr richtig ausbreiten – das Signal für den Informationsabgleich fehlt deshalb in den entsprechenden Hirnbereichen“, fasst Marc Aurel Busche zusammen.
Den Wissenschaftlern gelang es auch auf molekularer Ebene diesen Defekt zu entschlüsseln: Damit sich die Wellen korrekt ausbreiten können, muss eine präzise Balance zwischen Anregung und Hemmung auf Nervenzellen eingehalten werden. Bei den Alzheimer-Mäusen kam dieses Gleichgewicht durch die Proteinablagerungen durcheinander – die Hemmung war vermindert.
Geringe Dosen Schlafmittel als mögliche Therapie
Dieses Wissen nutzten Busche und sein Team, um den Defekt medikamentös zu behandeln. Von einer Sorte Schlafmitteln, den Benzodiazepinen, ist bekannt, dass sie die hemmenden Einflüsse im Gehirn verstärken. Verabreichten die Wissenschaftler geringe Mengen des Schlafmittels den Mäusen (etwa ein Zehntel einer Standarddosis), konnten sich auch die langsamen Schlafwellen wieder korrekt ausbreiten. Dass nun auch die Lernleistung wieder besser war, zeigten sie anschließend bei den Tieren mit Verhaltensexperimenten.
Für die Forscher sind die Ergebnisse natürlich erst ein Anfang auf dem Weg zu einer geeigneten Therapie gegen Alzheimer. „Diese Erkenntnisse sind aber aus zwei Gründen hochinteressant: erstens haben Mäuse und Menschen dieselben Schlafoszillationen im Gehirn – die Ergebnisse sind also übertragbar. Zweitens lassen sich diese Wellen mit einem normalen EEG-Gerät erfassen und somit auch Störungen schon früh diagnostizieren“, fasst der Wissenschaftler zusammen.
Publikation
Marc Aurel Busche, Maja Kekuš, Helmuth Adelsberger, Takahiro Noda, Hans Förstl, Israel Nelken und Arthur Konnerth, Rescue of long-range circuit dysfunction in Alzheimer’s disease models, Nature Neuroscience, 12. Oktober, 2015.
DOI: 10.1038/nn.4137
Kontakt
Dr. Dr. Marc Aurel Busche
Klinik und Poliklinik für Psychiatrie und Psychotherapie am TUM Klinikum rechts der Isar &
Institut für Neurowissenschaften der TUM
Tel: +49 (0)89 4140 – 4201
aurel.busche@tum.de
Technische Universität München
Corporate Communications Center
- Dr. Vera Siegler
- vera.siegler@tum.de
- presse@tum.de
- Teamwebsite