Neue Details zur Hemmung des Immunoproteasoms als Basis für neue Medikamente
Autoimmunkrankheiten ausbremsen
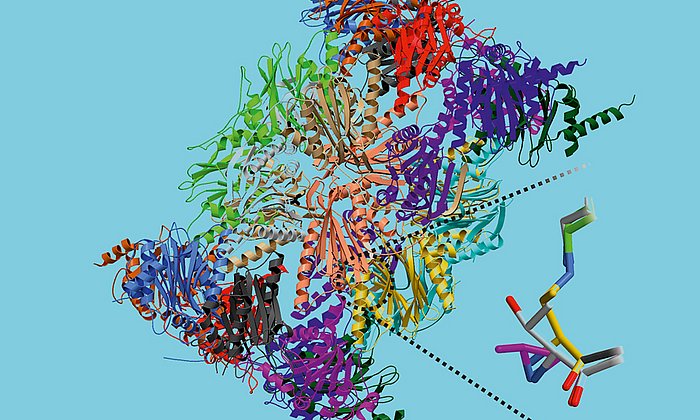
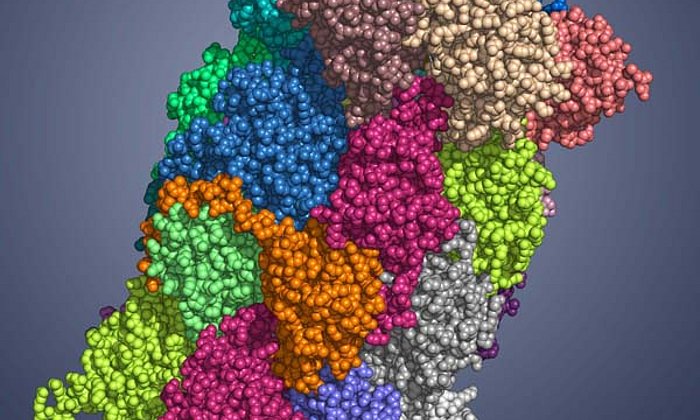
Das Immunsystem schützt den Körper vor Eindringlingen. Um jedoch zu erkennen, dass in einer betroffenen Zelle etwas nicht stimmt, braucht es „Informanten“ im Zellinneren, die ihm zeigen, welche Proteine gerade in der Zelle vorhanden sind. Diese wichtige Aufgabe übernimmt das Immunoproteasom, ein großer zylinderförmiger Proteinkomplex.
Es zerlegt Proteine und sorgt dafür, dass die Spaltprodukte an der Zelloberfläche präsentiert werden. So entsteht ein Abbild der im Zellinneren anwesenden Eiweiße, das regelmäßig vom Immunsystem überprüft wird. Identifiziert dieses eines der so präsentierten Bruchstücke als „fremd“, da es etwa von einem Virus stammt, vernichtet es die Zelle.
Ein außer Kontrolle geratener Helfer
Autoimmunerkrankungen wie Rheumatoide Arthritis, Diabetes Typ I oder Multiple Sklerose können beispielsweise durch die übermäßige Aktivität des Immunoproteasoms verursacht werden. Dies führt zu einer Entzündungsreaktion, die fälschlicherweise gesundes Gewebe angreift. Daher versuchen Wissenschaftler neue Wirkstoffe zu entwickeln, die gezielt das Immunoproteasom bremsen und so die ungewünschte Abwehrreaktion verhindern.
Besonders wichtig ist es dabei einen Wirkstoff zu finden, der ausschließlich das Immunoproteasom und nicht auch das ebenfalls in der Zelle vorhandene konstitutive Proteasom hemmt. Dieses ist für das Recyceln von defekten oder überflüssigen Proteinen zuständig und unterscheidet sich vom Immunoproteasom lediglich in den katalytischen Untereinheiten.
Eine Hemmung beider Proteasomtypen, wie es etwa das gegen Blutkrebs eingesetzte Medikament Bortezomib bewirkt, ist für die Zelle tödlich. Doch einen zugelassenen Hemmstoff, der selektiv nur das Immunoproteasom angreift, gibt es bisher nicht.
Der Weg zum gezielten Wirkstoff
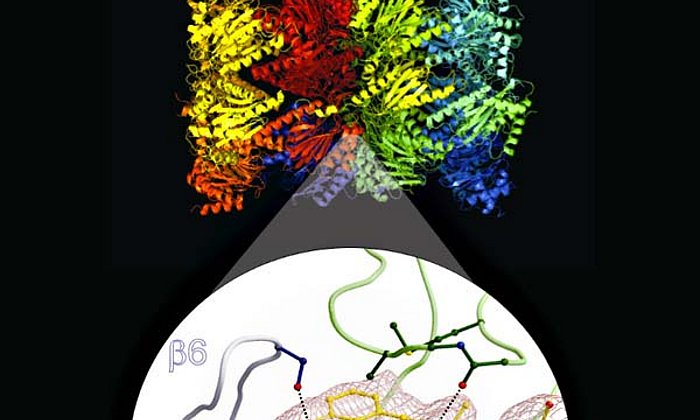
Nun ist es den Wissenschaftlern Dr. Eva Maria Huber, Dr. Wolfgang Heinemeyer und Prof. Michael Groll vom Lehrstuhl für Biochemie der Technischen Universität München in Zusammenarbeit mit Forschern des Leiden Institute of Chemistry gelungen, mittels Röntgenstrukturanalyse neue Bindemechanismen aufzudecken, die für die selektive Hemmung einer wichtigen Untereinheit des menschlichen Immunoproteasoms genutzt werden können.
„Bislang wussten wir zwar, dass bestimmte Wirkstoffe stärker am Immunoproteasom angreifen als am konstitutiven Proteasom, doch wir kannten den Grund dafür nicht“, erklärt Groll. „Das Verständnis darüber, wie unterschiedliche Hemmstoffe an beiden Proteasomtypen binden ermöglicht es nun, Inhibitoren mit größerer Selektivität und Wirksamkeit zu entwickeln“.
Auch den Grund, warum manche Inhibitoren an das menschliche Immunoproteasom besser binden als an das Immunoproteasom der Maus konnten die Forscher aufklären: „Eine einzige Aminosäure, in der sich die beiden Spezies unterscheiden, führt dazu, dass sich der Wirkstoff bei der Maus ‘verklemmt‘, beim Menschen jedoch ohne Widerstand andocken kann. Diese Erkenntnis ist wichtig für die Pharmaindustrie, denn sie legt nahe, bestimmte Inhibitoren nicht an Mäusen zu testen“, berichtet Huber.
Ein menschliches Protein in Hefe – eine langjährige Arbeit trägt Früchte
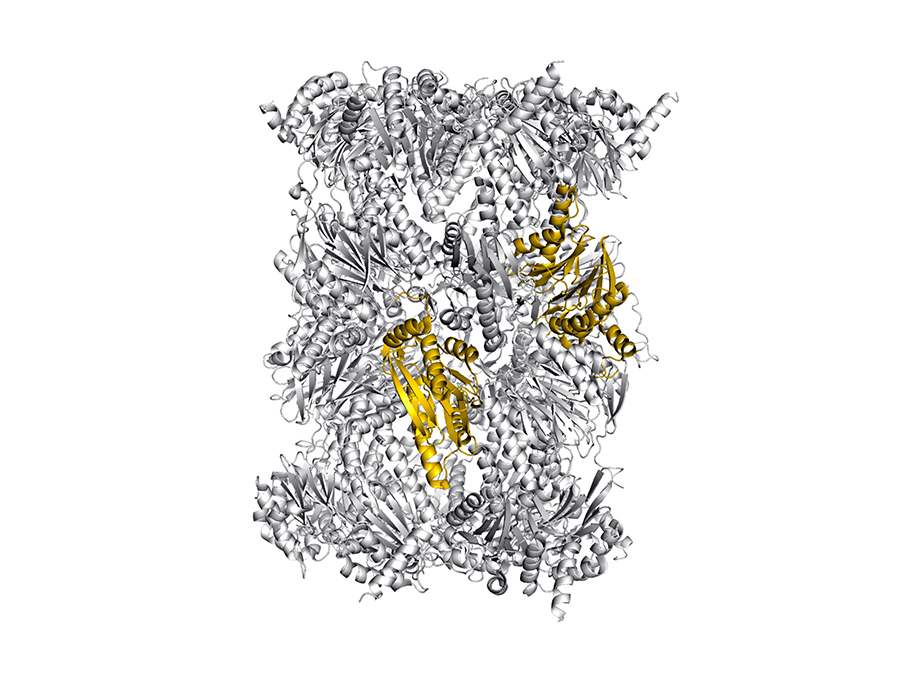
In ihrer Arbeit stellen die Forscher eine neue Methode vor, das menschliche Immunoproteasom, das sonst nur schwer zu isolieren ist, strukturell zu untersuchen: Sie bauten die für die Inhibitor-Bindung wesentlichen Sequenzen des menschlichen Immunoproteasoms in das Proteasom von Hefezellen ein – eine Technik, die 23 Jahre zurückliegende Versuche aufgreift, ganze Immunoproteasom-Untereinheiten ins Hefeproteasom einzusetzen.
„Die dabei entstandenen Mischproteine, die sich aus Sequenzstücken von Hefe und Mensch zusammensetzen und sich leicht in großen Mengen in Hefezellen herstellen lassen, sind dem natürlichen Immunoproteasom strukturell erstaunlich ähnlich“, sagt Heinemeyer. „Wir haben damit ein Modell geschaffen, mit dem neue Inhibitoren bestens untersucht werden können“.
Ein Hemmstoff, dessen Kernstruktur ebenfalls Gegenstand der Forschung von Wissenschaftlern um Prof. Groll war, wird bereits in klinischen Studien an Probanden getestet. Die nun neu gewonnenen Erkenntnisse eröffnen zusätzliche Möglichkeiten in Zukunft potentielle Wirkstoffe weiter zu verbessern.
Die Forschungsarbeiten wurden mit Mitteln des Exzellenzclusters Center for Integrated Protein Science Munich (CIPSM), der Deutschen Forschungsgemeinschaft sowie der Peter und Traudl Engelhorn-Stiftung unterstützt. Die Röntgenstrukturdaten wurden an der Synchrotron-Strahlungsquelle des Paul Scherrer Instituts (Villigen, Schweiz) ermittelt.
Originalpublikation:
Eva M Huber, Wolfgang Heinemeyer, Gerjan de Bruin, Herman S Overkleeft und Michael Groll. A humanized yeast proteasome identifies unique binding modes of inhibitors for the immunosubunit ß5i. The EMBO Journal (2016) e201695222 - DOI: 10.15252/embj.201695222
Kontakt:
Prof. Dr. Michael Groll
Lehrstuhl für Biochemie
Technische Universität München
Lichtenbergstr. 4
85748 Garching
Tel: +49 89 289 13361
michael.groll@tum.de
Technische Universität München
Corporate Communications Center
- Dr. Andreas Battenberg
- battenberg@zv.tum.de
- presse@tum.de
- Teamwebsite