Melanin als neuer Diagnose- und Behandlungsansatz für Tumore
Schwarze Nanopartikel bremsen Tumorwachstum

Nanopartikel gelten als vielversprechender Ansatz für die Tumorbekämpfung, weil Tumorgewebe sie aufgrund eines durchlässigeren Blutgefäßsystems leichter aufnimmt als gesunde Zellen. Ein Beispiel für sie sind kleine Bläschen, die von Bakterienmembran umgeben sind und als "Outer Membrane Vesicles“ (OMVs) bezeichnet werden. Die 20 – 200 Nanometer großen Partikel haben viele Vorteile: Sie sind biologisch verträglich und abbaubar, lassen sich leicht und günstig auch in großem Maßstab in Bakterien produzieren, zum Beispiel mit medikamentösen Wirkstoffen beladen und einfach verabreichen.
Nanopartikel mit schwarzer Fracht
Welches große Potential OMVs noch für die Tumordiagnostik und -therapie haben können, hat Prof. Vasilis Ntziachristos, Professor für Biologische Bildgebung an der TUM, mit seinem Team gezeigt. Sie nutzten dabei die charakteristischen Eigenschaften von OMVs und Melanin.
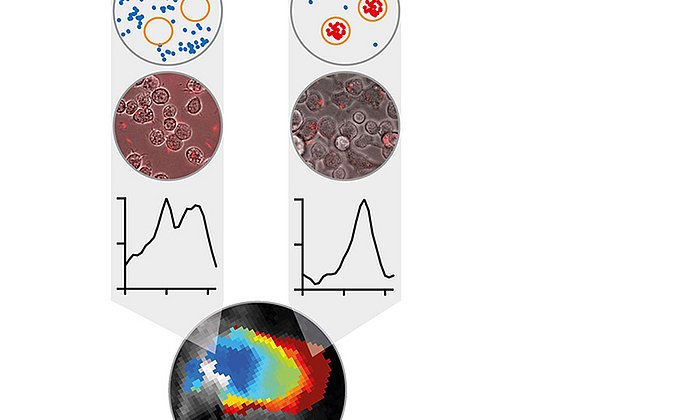
Dr. Vipul Gujrati, Erstautor der Studie, erklärt das Prinzip: „Melanin absorbiert Licht sehr gut - auch im Infrarot-Bereich. Genau dieses Licht nutzen wir in unserem bildgebenden Verfahren Optoakustik für die Tumordiagnostik. Gleichzeitig setzt Melanin diese aufgenommene Energie in Wärme um, die es wieder abstrahlt. Und Wärme wird in ersten klinischen Studien für die Tumorbekämpfung eingesetzt“.
Die Optoakustik kombiniert die Vorteile von optischer Bildgebung und Ultraschalltechnik und wurde von Ntziachristos entscheidend vorangebracht. Dabei erwärmen schwache Laserimpulse das Gewebe geringfügig, woraufhin es sich minimal und kurzzeitig ausdehnt. Zieht sich das Gewebe in Folge der Abkühlung wieder zusammen entstehen Ultraschallsignale. Je nach Art des Gewebes unterscheiden sich die gemessenen Signale. Diese erfassen die Wissenschaftlerinnen und Wissenschaftler dann mit entsprechenden Detektoren und ‚übersetzen‘ sie in dreidimensionale Bilder. Mit Hilfe von Sensormolekülen lässt sich die Spezifizität und Genauigkeit der Technik noch weiter steigern.
Wärmeentwicklung reduziert Tumorwachstum
Das Team hatte aber zuerst ein Problem zu lösen: Melanin ist schlecht wasserlöslich und damit schwer zu verabreichen. Hier kamen die OMVs ins Spiel: Die Forscherinnen und Forscher veränderten Bakterien so, dass sie Melanin produzieren und in ihre Membran und den daraus entstehenden Nanopartikeln einlagern konnten. Sie testeten die schwarzen Nanopartikel anschließend in Mäusen, die Tumore im Brustbereich hatten. Die Partikel wurden direkt in den Tumor gespritzt und dieser mit Infrarot-Laserimpulsen im Zuge der optoakustischen Untersuchung angeregt.
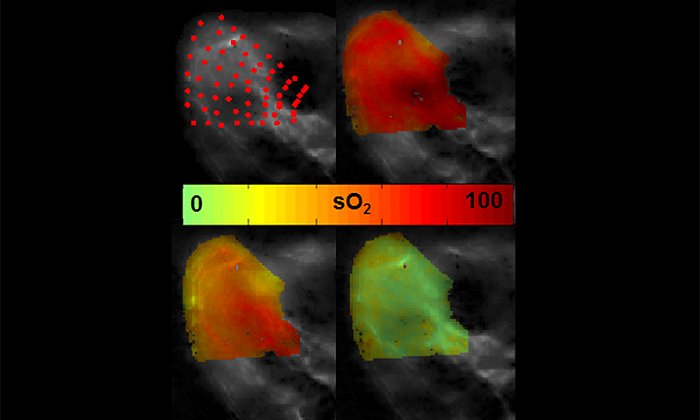
Es zeigte sich, dass sich die OMVs als Sensormoleküle für diese Diagnosetechnik eigneten, weil sie kontrastreiche und scharfe Bilder des Tumors lieferten. Zudem waren sie auch für photothermale Therapieansätze einsetzbar, bei denen das Tumorgewebe mit stärkeren Laserimpulsen erhitzt wird, so dass die Krebszellen absterben. Durch das Melanin erwärmte sich das Tumorgewebe von 37°C auf bis zu 56°C, während Kontrolltumore ohne Melanin sich nur auf bis zu 39°C erwärmten. Im Verlauf von zehn Tagen nach der Behandlung wuchsen die Tumore deutlich langsamer als in der Kontrollgruppe, die keine Melanin-OMVs erhalten hatten. Verstärkt wurde diese Wärmewirkung durch einen weiteren positiven Effekt der Partikel: sie verursachten eine leichte unspezifische Entzündung im Tumorgewebe, was das Immunsystem anregte, den Tumor zu bekämpfen.
„Unsere Melanin-Nanopartikel sind ‚Theranostics‘ – sie könnten gleichzeitig diagnostisch und therapeutisch eingesetzt werden. Das macht sie hochinteressant für die klinische Anwendung“, sagt Vasilis Ntziachristos. Das Team möchte nun ihre OMVs weiterentwickeln, so dass sie künftig auch klinisch genutzt werden können.
Publikation:
Vipul Gujrati, Jaya Prakash, Jaber Malekzadeh-Najafabadi, Andre Stiel, Uwe Klemm, Gabriele Mettenleiter, Michaela Aichler, Axel Walch and Vasilis Ntziachristos: Bioengineered bacterial vesicles as biological nanoheaters for optoacoustic imaging, Nature Communications, March 7, 2019, DOI: 10.1038/s41467-019-09034-y
Mehr Informationen:
Prof. Vasilis Ntziachristos ist Lehrstuhlinhaber an der TUM, Forschungsgruppenleiter am Zentralinstitut für Translationale Krebsforschung der TUM (TranslaTUM) und Direktor des Instituts für Biologische und Medizinische Bildgebung am Helmholtz Zentrum München.
Kontakt:
Dr. Vipul Gujrati
Wissenschaftler am Lehrstuhl für Biologische Bildgebung
Technische Universität München
Tel.: +49 (0)89 3187 - 1244
vipul.gujrati@tum.de
Technische Universität München
Corporate Communications Center
- Dr. Vera Siegler
- vera.siegler@tum.de
- +49 (0)89 23325
- presse@tum.de
- Teamwebsite