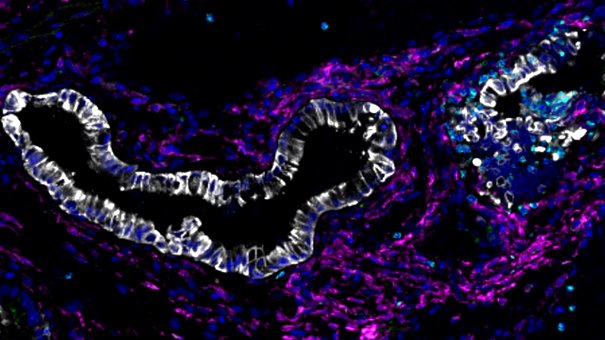
Wie identische Gen-Mutationen unterschiedliche Krebsarten auslösen
Gewebetyp beeinflusst die Krebs-Entwicklung

Die Behandlung von Bauchspeicheldrüsen- und Gallengangkrebs hat sich in den letzten Jahrzehnten nicht wesentlich verbessert. Bis heute gibt es keine wirksamen zielgerichteten Therapien. „Die Situation für Patienten mit Bauchspeicheldrüsen- und extrahepatischem Gallengangkrebs ist immer noch sehr bedrückend, nur etwa zehn Prozent der Betroffenen überleben fünf Jahre“, sagt Dieter Saur, Professor für Translationale Krebsforschung an der Technischen Universität München (TUM). Saur ist einer der Wissenschaftler und Wissenschaftlerinnen am Partnerstandort München des Deutschen Konsortiums für translationale Krebsforschung (DKTK) am Universitätsklinikum rechts der Isar. Mit einem Team aus Forscherinnen und Forschern von TUM, DKTK und Universitätsmedizin Göttingen hat er die Enstehung der beiden Krebsarten genauer untersucht.
„Um neue therapeutische Ansätze zu entdecken, die die Prognose dieser Patientinnen und Patienten verbessern, müssen wir dringend die gewebespezifischen genetischen Netzwerke verstehen, die diese Tumoren steuern. Das kann uns dabei helfen, in Zukunft präzisere Therapien einzusetzen,“ sagt Dieter Saur.
Unerwartete Ergebnisse
Das Team untersuchte die Entwicklung von Gallengangs- und Bauchspeicheldrüsenkrebs in Mäusen, bei denen die Onkogene PIK3CA und KRAS durch mutierte Versionen ersetzt wurden. Diese Mutationen waren mit denen identisch, die die beiden Krebsarten beim Menschen antreiben. Die Expression der mutierten Onkogene in den gemeinsamen Vorläuferzellen des Gallengangs und in der Bauchspeicheldrüse führte zu sehr unterschiedlichen Ergebnissen. Mäuse mit dem mutierten PI3K-Gen entwickelten überwiegend Gallengangkrebs, Mäuse mit dem mutierten KRAS-Gen dagegen ausschließlich Bauchspeicheldrüsenkrebs.
Dies war unerwartet, da beide Gene in beiden menschlichen Krebsarten mutiert sind. Weitere Analysen des Teams deckten die zugrundeliegenden genetischen Prozesse auf, die zu der unterschiedlichen Empfindlichkeit gegenüber den krebstreibenden Mutationen führen.
Molekulare Prozesse aufgedeckt
„Unsere Studien an Mäusen haben gezeigt, wie Gene zusammenarbeiten, um Krebs in verschiedenen Organen zu verursachen. Wir haben die Hauptakteure identifiziert, die Reihenfolge, in der sie während der Tumorprogression auftreten, und die molekularen Prozesse, die normale Zellen in gefährliche Krebszellen verwandeln. Solche Prozesse sind potenzielle Ziele für neue Behandlungen“, sagt Chiara Falcomatà, Erstautorin der aktuellen Publikation.
In den Mäusen konnte das Team genetische Programme identifizieren, die die Entwicklung der beiden Krebsarten vorantreiben. So kooperieren beispielsweise verschiedene genetische Ereignisse und überaktivieren dadurch den PI3K-Signalweg, was die Zellen bösartig entarten lässt. Andere Mutationen setzten regulatorische Proteine außer Kraft, so dass sie ihre Fähigkeit verlieren, das Fortschreiten der Erkrankung zu bremsen.
Signalnetzwerke machen anfällig für Krebs
„Das Verständnis der genetischen Wechselwirkungen in verschiedenen Krebsarten kann in Zukunft zu präziseren therapeutischen Entscheidungen führen“, sagt Günter Schneider, Professor für Translationale Krebsforschung an der Universitätsmedizin Göttingen.
„Was wir gezeigt haben, ist, dass die Funktion eines Onkogens abhängt vom Gewebetyp und davon, welche anderen Gene verändert sind“, sagt Roland Rad, Professor für Molekulare Onkologie und Funktionelle Genomik an der TUM und DKTK-Forscher. „Damit es zur Krebsentstehung kommt, müssen diese Onkogene das intrinsische Signalnetzwerk eines bestimmten Gewebes kapern. Interessanterweise existieren solche Netzwerke nur in bestimmten Gewebetypen, die dadurch anfällig für die Krebsentstehung sind.“
„Kein einzelnes Gen kann Therapieerfolg vorhersagen“
Diese Erkenntnisse des Teams um Saur, Schneider und Rad haben wichtige Implikationen für therapeutische Interventionen. „Das Konzept, dass gewebespezifische genetische Interaktionen die Krebsentwicklung vorantreiben, zeigt, dass kein einzelnes Gen das Ansprechen einer Krebserkrankung auf eine bestimmte Therapie vorhersagen kann“, sagt Saur.„Um die Präzisionsmedizin auf die nächste Stufe zu heben, müssen wir in Zukunft besser verstehen, welche gewebespezifischen Determinanten ein therapeutisches Ansprechen oder eine Resistenz bestimmen.“
Mehrere der Autoren der aktuellen Studie, darunter Dieter Saur und Roland Rad, sind am TranslaTUM, dem Zentrum für Translationale Krebsforschung der TUM, angesiedelt. In diesem interdisziplinären Forschungsinstitut erforschen Medizinerinnen und Mediziner gemeinsam mit Kolleginnen und Kollegen aus den Natur- und Ingenieurwissenschaften die Ursachen und Behandlungsmöglichkeiten von Krebserkrankungen.
C. Falcomatà, S. Bärthel, A. Ulrich, S. Diersch, C. Veltkamp, L. Rad, F. Boniolo, M. Solar, K. Steiger, B. Seidler, M. Zukowska, J. Madej, M. Wang, R. Öllinger, R. Maresch, M. Barenboim, S. Eser, M. Tschurtschenthaler, A. Mehrabi, S. Roessler, B. Goeppert, A. Kind, A. Schnieke, M. S. Robles, A. Bradley, R. M. Schmid, M. Schmidt-Supprian, M. Reichert, W. Weichert, O. J. Sansom, J. P. Morton, R. Rad, G. Schneider, D. Saur. "Genetic screens identify a context-specific PI3K/p27Kip1 node driving extrahepatic biliary cancer". Cancer Discovery 2021, DOI: 10.1158/2159-8290.CD-21-0209
- Website des TranslaTUM
- Im Deutschen Konsortium für translationale Krebsforschung (DKTK) interagiert das Deutsche Krebsforschungszentrum (DKFZ) in Heidelberg als Kernzentrum langfristig mit onkologisch besonders ausgewiesenen universitären Partnerstandorten in Deutschland.
Technische Universität München
Corporate Communications Center
- Paul Hellmich
- paul.hellmich@tum.de
- presse@tum.de
- Teamwebsite
Kontakte zum Artikel:
Prof. Dr. Dieter Saur
Technische Universität München
Professor für Translationale Tumorforschung
dieter.saur@tum.de